CONFIGURACIÓN ELECTRÓNICA
Al referirnos a la configuración electrónica (o periódica) estamos hablando de la descripción de la ubicación de los electrones en los distintos niveles (con subniveles y orbitales) de un determinado átomo.
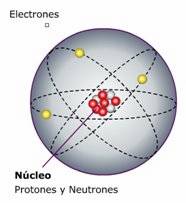
Modelo atómico general.
Configurar significa "ordenar" o "acomodar", y electrónico deriva de "electrón"; así, configuración electrónica es la manera ordenada de repartir los electrones en los niveles y subniveles de energía.
Científicamente, diremos que es la representación del modelo atómico de Schrödinger o modelo de la mecánica cuántica. En esta representación se indican los niveles, subniveles y los orbitales que ocupan los electrones.
Debemos acotar que aunque el modelo de Schrödinger es exacto sólo para el átomo de hidrógeno, para otros átomos es aplicable el mismo modelo mediante aproximaciones muy buenas.
Para comprender (visualizar o graficar) el mapa de configuración electrónica (o periódica) es necesario revisar los siguientes conceptos.
Los Números Cuánticos
En el contexto de la mecánica cuántica, en la descripción de un átomo se sustituye el concepto de órbita por el de orbital atómico. Un orbital atómico es la región del espacio alrededor del núcleo en el que la probabilidad de encontrar un electrón es máxima.
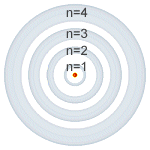 |
| Número cuántico principal (n). |
La solución matemática de la ecuación de Schrödinger precisa de tres números cuánticos. Cada trío de valores de estos números describe un orbital.
Número cuántico principal (n): puede tomar valores enteros (1, 2, 3, 4, 5, 6, 7) y coincide con el mismo número cuántico introducido por Bohr. Está relacionado con la distancia promedio del electrón al núcleo en un determinado orbital y, por tanto, con el tamaño de este e indica el nivel de energía.
Número cuántico secundario (l): Los niveles de energía, identificados con el número cuántico principal (n), poseen subniveles, los cuales se asocian, además, a la forma del orbital, y son identificados por el número cuántico secundario (l). Entonces, los valores del número cuántico secundario dependen del número cuántico principal "n".
Así, la cantidad de subniveles de energía que posea cada nivel principal está dada por la fórmula n – 1 (el valor del número cuántico principal menos uno).
Este número cuántico secundario (l) nos indica en que subnivel se encuentra el electrón, y toma valores desde 0 hasta (n - 1), recordando que n es el valor del número cuántico principal. Así, para cada nivel n, el número cuántico secundario (l) será:
l = 0, 1, 2, 3,…, n-1.
Ejemplo:
Si n = 1 (n – 1 = 0), entonces l = 0 (en el nivel de energía 1 no hay subniveles de energía, y para efectos de comprensión se considera este nivel 1 como subnivel 0)
Si n = 2 (n -1 = 1), entonces l = 0, 1. El nivel de energía 2 posee dos subniveles, identificados como 0 y 1
Si n = 3 (n – 1 = 2), entonces l = 0, 1, 2. El nivel de energía 3 posee tres subniveles, identificados como 0, 1 y 2
Si n = 4 (n – 1 = 3), entonces l = 0, 1, 2, 3. El nivel de energía 4 posee cuatro subnoiveles, identificados como 0, 1, 2 y 3
Si n = 5 (n – 1 = 4), entonces l = 0, 1, 2, 3, 4. El nivel de energía 5 posee cinco subnoveles, identificados como 0, 1, 2, 3 y 4
También para efectos de comprensión, la comunidad científica ha aceptado que los números que representan los subniveles (0, 1, 2, y 3) sean reemplazados por las letras s, p, d y f, respectivamente, para representar los distintos tipos de orbitales.
Estas letras se optiene de la inicial de las palabras sharp (s), principal (p), difuso (d) y fundamental (f).
Cada subnivel, a su vez, posee distinta cantidad de orbitales, lo cual veremos más adelante.
Ahora, con respecto a la forma del orbital de estos subniveles, el número cuántico secundario (o azimutal) determina laexcentricidad de la órbita: cuanto mayor sea este número, más excéntrica será la órbita; es decir, será más aplanada la elipse que recorre el electrón.
Así, en el nivel 1 (o capa K) el valor del nivel (identificado como subnivel 0) es cero (no hay excentricidad) y su órbita es circular.
Cada vez que aumenta el valor del número cuántico secundario (o azimutal) aumenta la excentricidad de la órbita, como se demuestra en el siguiente gráfico:
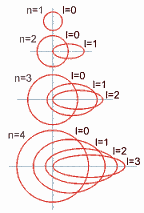 |
Número cuántico magnético (ml): puede tener todos los valores desde – l hasta + l pasando por cero. Describe la orientación espacial del orbital e indica el número de orbitales presentes en un subnivel determinado.
Para explicar determinadas características de los espectros de emisión se consideró que los electrones podían girar en torno a un eje propio, bien en el sentido de las agujas del reloj o en el sentido contrario. Para caracterizar esta doble posibilidad se introdujo elnúmero cuántico de espín (ms) que toma los valores de + ½ o – ½..
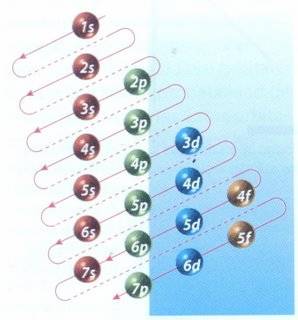 |
| Cuadro de las diagonales, mecanismo para distribuir electrones en sus diferentes niveles de energía. |
Para entender el concepto de configuración electrónica es necesario asumir o aplicar dos principios importantes:
• Principio de Incertidumbre de Heisenberg: “Es imposible determinar simultáneamente la posición exacta y el momento exacto del electrón”
• Principio de Exclusión de Pauli: “Dos electrones del mismo átomo no pueden tener los mismos números cuánticos idénticos y por lo tanto un orbital no puede tener más de dos electrones”.
Tipos de configuración electrónica
Para graficar la configuración electrónica existen cuatro modalidades, con mayor o menor complejidad de comprensión, que son:
Configuración estándar
Se representa la configuración electrónica que se obtiene usando elcuadro de las diagonales (una de sus formas gráficas se muestra en la imagen de la derecha).
Es importante recordar que los orbitales se van llenando en el orden en que aparecen, siguiendo esas diagonales, empezando siempre por el 1s.
Aplicando el mencionado cuadro de las diagonales la configuración electrónica estándar, para cualquier átomo, es la siguiente:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d10 7p6
Más adelante explicaremos cómo se llega este enjambre de números y letras que perturba inicialmente, pero que es de una simpleza sorprendente.
Configuración condensada
Los niveles que aparecen llenos en la configuración estándar se pueden representar con un gas noble (elemento del grupo VIII A,Tabla Periódica de los elementos), donde el número atómico del gas coincida con el número de electrones que llenaron el último nivel.
Los gases nobles son He, Ne, Ar, Kr, Xe y Rn.
Configuración desarrollada
Consiste en representar todos los electrones de un átomo empleando flechas para simbolizar el spin de cada uno. El llenado se realiza respetando el principio de exclusión de Pauli y la Regla de máxima multiplicidad de Hund.
 |
| Figura de un átomo sencillo ilustrando lo indefinido de sus órbitas. |
Configuración semidesarrollada
Esta representación es una combinación entre la configuración condensada y la configuración desarrollada. En ella sólo se representan los electrones del último nivel de energía.
Niveles de energía o capas
Si repasamos o recordamos los diferentes modelos atómicos veremos que en esencia un átomo es parecido a un sistema planetario. El núcleo sería la estrella y los electrones serían los planetas que la circundan, girando eso sí (los electrones) en órbitas absolutamente no definidas, tanto que no se puede determinar ni el tiempo ni el lugar para ubicar un electrón (Principio de Incertidumbre de Heisenberg).
Los electrones tienen, al girar, distintos niveles de energía según la órbita (en el átomo se llama capa o nivel) que ocupen, más cercana o más lejana del núcleo. Entre más alejada del núcleo, mayor nivel de energía en la órbita, por la tendencia a intercambiar o ceder electrones desde las capas más alejadas.
Entendido el tema de las capas, y sabiendo que cada una de ellas representa un nivel de energía en el átomo, diremos que:
1. Existen 7 niveles de energía o capas donde pueden situarse los electrones para girar alrededor del núcleo, numerados del 1, el más interno o más cercano al núcleo (el que tiene menor nivel de energía), al 7, el más externo o más alejado del núcleo (el que tiene mayor nivel de energía).
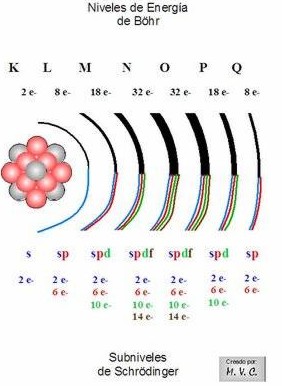
Estos niveles de energía corresponden al número cuántico principal (n) y además de numerarlos de 1 a 7, también se usan letras para denominarlos, partiendo con la K. Así: K =1, L = 2, M = 3, N = 4, O = 5, P = 6, Q = 7.
2. A su vez, cada nivel de energía o capa tiene sus electrones repartidos en distintos subniveles, que pueden ser de cuatro tipos: s, p, d, f.
Ilustración para los niveles y subniveles de energía electrónica en el átomo | |
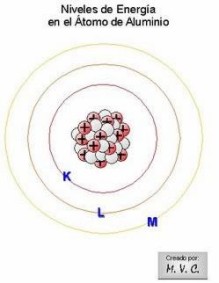 |  |
Imágenes tomadas de la página:
http://configraelectrones-mvc.blogspot.com/ | |
Para determinar la configuración electrónica de un elemento sólo hay que saber cuantos electrones debemos acomodar y distribuir en los subniveles empezando con los de menor energía e ir llenando hasta que todos los electrones estén ubicados donde les corresponde. Recordemos que partiendo desde el subnivel s, hacia p, d o f se aumenta el nivel de energía.
3. En cada subnivel hay un número determinado de orbitales que pueden contener, como máximo, 2 electrones cada uno. Así, hay 1 orbital tipo s, 3 orbitales p, 5 orbitales d y 7 del tipo f. De esta forma el número máximo de electrones que admite cada subnivel es: 2 en el s; 6 en el p (2 electrones x 3 orbitales); 10 en el d (2 x 5); 14 en el f (2 x 7)..
La distribución de niveles, subniveles, orbitales y número de electrones posibles en ellos se resume, para las 4 primera capas, en la siguiente tabla:
| Niveles de energía o capa (n) |
1 (K)
|
2 (L)
|
3 (M)
|
4 (N)
|
Tipo de subniveles
|
s
|
s p
|
s p d
|
s p d f
|
Número de orbitales en cada subnivel
|
1
|
1 3
|
1 3 5
|
1 3 5 7
|
Denominación de los orbitales
|
1s
|
2s 2p
|
3s 3p 3d
|
4s 4p 4d 4f
|
Número máximo de electrones en los orbitales
|
2
|
2 - 6
|
2 - 6 - 10
|
2 - 6 - 10 - 14
|
Número máximo de electrones por nivel de energía o capa
|
2
|
8
|
18
|
32
|
Insistiendo en el concepto inicial, repetimos que la configuración electrónica de un átomo es la distribución de sus electrones en los distintos niveles, subniveles y orbitales. Los electrones se van situando en los diferentes niveles y subniveles por orden de energía creciente (partiendo desde el más cercano al núcleo) hasta completarlos.
Recordemos que alrededor del núcleo puede haber un máximo de siete capas atómicas o niveles de energía donde giran los electrones, y cada capa tiene un número limitado de ellos.
La forma en que se completan los niveles, subniveles y orbitales está dada por la secuencia que se grafica en el esquema conocido como regla de las diagonales:
Es importante saber cuantos electrones existen en el nivel más externo de un átomo pues son los que intervienen en los enlaces con otros átomos para formar compuestos.
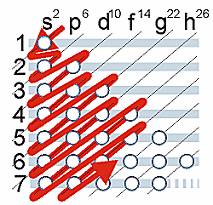 |
Regla de las diagonales
Sirve para determinar el mapa de configuración electrónica (o periódica) de un elemento.
En otras palabras, la secuencia de ocupación de los orbitales atómicos la podemos graficar usando la regla de la diagonal, para ello debemos seguir la flecha roja del esquema de la derecha, comenzando en 1s; siguiendo la flecha podremos ir completando los orbitales con los electrones en forma correcta.
En una configuración estándar, y de acuerdo a la secuencia seguida en el grafico de las diagonales, el orden de construcción para la configuración electrónica (para cualquier elemento) es el siguiente:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d10 7p6
Los valores que se encuentran como superíndices indican la cantidad máxima de electrones que puede haber en cada subnivel (colocando sólo dos en cada orbital de los subniveles).
La Tabla Periódica, punto de partida
 |
| El sodio en la tabla |
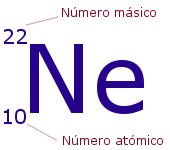
En la tabla periódica, entre los datos que encontramos de cada uno de los elementos se hallan elNúmero atómico y la Estructura electrónica o Distribución de electrones en niveles.
El Número atómico nos indica la cantidad de electrones y de protones que tiene un elemento.
La Estructura electrónica o Distribución de electrones en niveles indica cómo se distribuyen los electrones en los distintos niveles de energía de un átomo (lo que vimos más arriba con la regla de las diagonales).
Pero, si no tengo la tabla periódica para saber cuantos electrones tengo en cada nivel, ¿cómo puedo hacer para averiguarlo?
Ya vimo que la regla de las diagonales ofrece un medio sencillo para realizar dicho cálculo.
Para escribir la configuración electrónica de un átomo es necesario:
Saber el número de electrones que tiene el átomo; para ello basta conocer el número atómico (Z) del átomo en la tabla periódica. Recuerda que el número de electrones en un átomo neutro es igual al número atómico (Z).
Ubicar los electrones en cada uno de los niveles de energía, comenzando desde el nivel más cercano al núcleo (nivel 1).
Respetar la capacidad máxima de cada subnivel (s = 2e-, p = 6e-, d = 10e- y f = 14e-).
Supongamos que tenemos que averiguar la Distribución electrónica en el elemento sodio, que como su número atómico indica tiene 11 electrones, los pasos son muy sencillos: debemos seguir las diagonales, como se representan más arriba.
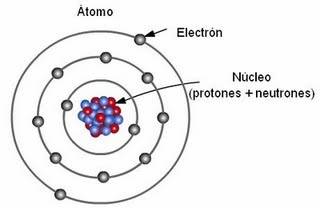 |
| Ilustración simplificada de un átomo. |
En el ejemplo del sodio sería: 1s2, como siguiendo la diagonal no tengo nada busco la siguiente diagonal y tengo 2s2, como siguiendo la diagonal no tengo nada busco la siguiente diagonal y tengo 2p6, siguiendo la diagonal tengo 3s2.
Siempre debo ir sumando los superíndices, que me indican la cantidad de electrones. Si sumo los superíndices del ejemplo, obtengo 12, quiere decir que tengo un electrón de más, ya que mi suma para ser correcta debe dar 11, por lo que al final debería corregir para que me quedara 3s1.
Por lo tanto, para el sodio (11 electrones), el resultado es: 1s2 2s2 2p6 3s1
Primer nivel: 2 electrones (los 2 en subnivel s, en un orbital);
Segundo nivel: 8 electrones (2 en subnivel s, en un orbital, y 6 en subnivel p, con 2 en cada uno de sus 3 orbitales);
tercer nivel: 1 electrón (ubicado en el subnivel s, en un orbital).
;
En la tabla periódica podemos leer, respecto al sodio: 2 - 8 - 1
Otros ejemplos:
CLORO: 17 electrones
1s2 2s2 2p6 3s2 3p5
1º nivel: 2 electrones
2º nivel: 8 electrones 3º nivel: 7 electrones En la tabla periódica podemos leer: 2 - 8 - 7 |
MANGANESO: 25 electrones
1s2 2s2 2p6 3s2 3p6 4s2 3d5
1º nivel: 2 electrones
2º nivel: 8 electrones 3º nivel: 13 electrones 4º nivel: 2 electrones En la tabla periódica podemos leer: 2 - 8 - 13 – 2 |
El superíndice es el número de electrones de cada subnivel (recordando siempre que en cada orbital del subnivel caben solo dos electrones).
El Número máximo de electrones por nivel es 2(n)2 (donde n es la cantidad de subniveles que tiene cada nivel).
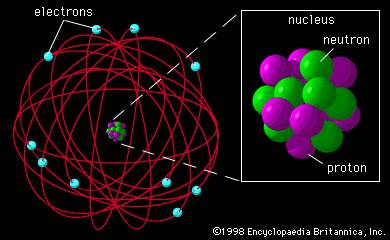 |
| Ilustración más compleja y más realista de la estructura de un átomo. |
Hagamos un ejercicio:
Supongamos que deseamos conocer la configuración electrónica de la plata, que tiene 47 electrones.
Por lo ya aprendido, sabemos que el orden de energía de los orbitales es 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, etc.
En cada subnivel s (que tienen sólo un orbital) cabrán dos electrones.
En cada subnivel p (que tienen 3 orbitales) cabrán 6 electrones.
En cada subnivel d (que tienen 5 orbitales) cabrán 10 electrones.
En cada subnivel f (que tienen 7 orbitales) cabrán 14 electrones.
Siguiendo esta regla debemos colocar los 47 electrones del átomo de plata, la cual debe quedar así::
1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d9
donde sólo se han puesto 9 electrones en los orbitales d (que son cinco) de la capa cuarta para completar, sin pasarse, los 47 electrones de la plata.
Otro ejemplo:
Configuración electrónica del fósforo (P)
Nº atómico Z = 15
15 protones y 15 electrones
1s2 2s2 2p6 3s2 3p3
Relación de la Configuración electrónica con la Tabla Periódica
De modo inverso, si tenemos o conocemos la configuración electrónica de un elemento podemos predecir exactamente el número atómico, el grupo y el período en que se encuentra el elemento en la tabla periódica.
Por ejemplo, si la configuración electrónica de un elemento es 1s2 2s2 2p6 3s2 3p5, podemos hacer el siguiente análisis:
Para un átomo la suma total de los electrones es igual al número de protones; es decir, corresponde a su número atómico, que en este caso es 17. El período en que se ubica el elemento está dado por el máximo nivel energético de la configuración, en este caso corresponde al período 3, y el grupo está dado por la suma de los electrones en los subniveles s y p del último nivel; es decir, corresponde al grupo 7.
-sulfide-unit-cell-3D-balls.png)